Introduction

Avis du pôle scientifique Médiamphi
Pastille orange
Pastille orange
Cette revue systématique est un article à risque de biais modéré. En effet, la qualité des articles est bien évaluée par les auteurs mais ils n’en tiennent pas compte dans l’interprétation des résultats. Les résultats peuvent par conséquent être sûrs ou sous-estimés, ne reflétant pas la réalité.
L’hyperhydratation est commune dans les ultra-trails et peut entraîner une hyponatrémie liée à l’exercice (EAH = exercise-associated hyponatremia). L’EAH est définie comme une trop faible concentration de sodium (<135mmol/L) pouvant durer jusqu’à 24 heures post-effort et elle est classifiée en 3 stades en fonction de la concentration de sodium : faible (entre 130 et 135 mmol/L), moyenne (entre 125 et 129 mmol/L) et forte (<125 mmol/L). Elle présente de nombreux symptômes tels que des nausées, vertiges, une augmentation de la pression intracrânienne, une perte de connaissance allant parfois jusqu’à la mort. L’hyperhydratation pendant les ultra-trails est la cause primaire de l’EAH dont l’incidence varie de 4 à 50% chez les coureurs d’ultramarathon en fonction des caractéristiques de la course. L’EAH peut entrainer une diminution du taux de filtration glomérulaire et donc une diminution de la capacité à diluer l’urine et à relâcher l’eau libre, ce qui peut amener à une insuffisance rénale aigue (AKI = Acute Kidney Injury).
La déshydratation peut survenir de façon égale à l’hyperhydratation lors d’ultra-trails et pourra aussi être la cause d’une AKI. L’AKI est définie par une diminution brutale de la filtration glomérulaire, entrainant une augmentation de la concentration sanguine de produits nitrogénés qui peut être la cause de dommages structurels ou d’une perte de fonction des reins. Le diagnostic de l’AKI repose sur l’analyse des changements dans la concentration du sérum en créatinine (SCR) ou sur l’analyse des rejets urinaires.
L’AKI et l’EAH sont fréquemment présentes chez les patients hospitalisés et elles augmentent les risques de comorbidités. En revanche, il n’y a actuellement pas de données sur leur présence simultanée chez les coureurs d’ultra-trails et leurs effets sur la santé. L’objectif de cette étude sera donc d’observer l’incidence de ces deux pathologies dans les sports d’ultra-endurance en fonction des caractéristiques des courses ainsi que leur impact sur la santé des athlètes.
Méthode
Cette revue de littérature a inclus tous les articles relevant de l’EAH et de l’AKI dans l’ultra-trail depuis 15 ans (jusqu’au 31 Décembre 2021). Ils proviennent des bases de données PudMed, EBSCO, Web of Science et Alcorze.
-
Études de cas, études longitudinales, études observationnelles et études prospectives
-
Population adulte, des deux sexes
-
Courses de plus de 42km en milieu naturel, avec une ou plusieurs étapes
-
Analyses des biomarqueurs relatifs à l’AKI et à l’EAH
Les critères d’exclusions étaient principalement des durées de courses trop courtes, sans dénivelés, les sports combinés tels que le biathlon ou le triathlon et la présence chez les participants d’une pathologie rénale chronique.
Deux examinateurs ont relevé pour chaque étude : l’âge et le sexe des participants, les données sur la course (distance, dénivelé et nombre d’étapes), les conditions environnementales (température et degrés d’humidité), la masse corporelle et ses variations, les concentrations en créatinine pré et post-effort, l’estimation du taux de filtration glomérulaire, les critères utilisés pour la classification de l’AKI ainsi que sa sévérité, l’EAH pré et post-effort et sa sévérité.
Résultats
Au total, 28 études (descriptives pour la majorité) sur 30 ultra-trails différents ont été incluses dans cette revue systématique. Parmi ces articles, 13 rapportaient des résultats sur l’AKI, 15 sur l’EAH et 9 sur la combinaison AKI + EAH. Les tableaux suivants résument les données sur les participants, les courses et les incidences de l’AKI, de l’EAH et des deux combinées.
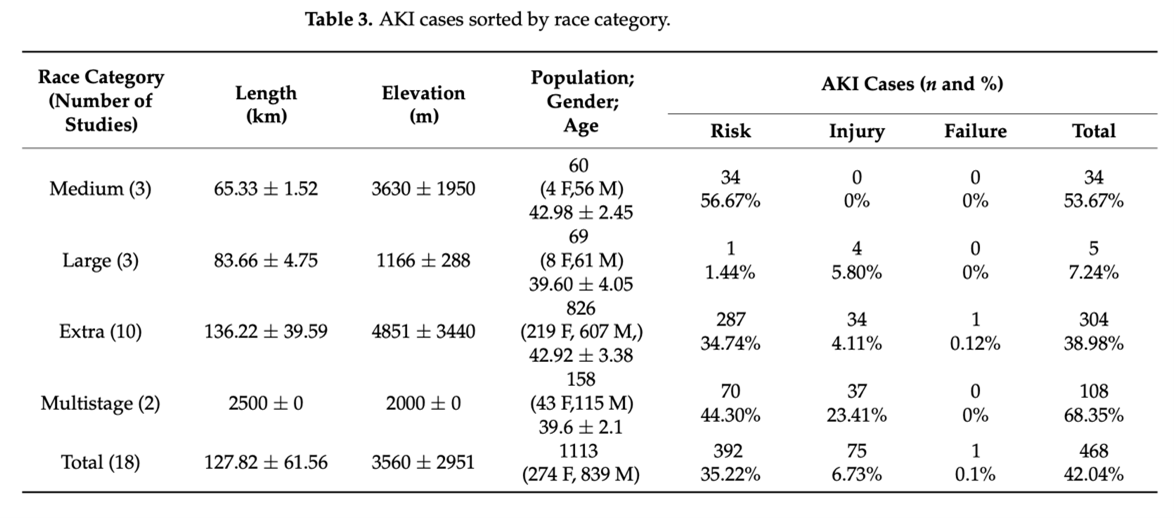
L’AKI a été évaluée par deux biomarqueurs : les niveaux SCR pré et post-course et l’analyse de la Cystatin C. Le nombre total de cas d’AKI était de 468 et son incidence était de 42,08%. La sévérité de l’AKI a été déterminée en utilisant les critères AKIN (Acute Kidney Injury Network), KDIGO (Kidney Disease : Improving Global Outcomes) ou RIFLE (Risk, Injury, Failure, Loss, End-stage). 392 participants ont présenté une AKI à stade précoce, 75 ont atteint le stade de blessure et seulement 1 participant a atteint le stade « d’échec ». 5 études évaluant l’AKI n’ont pas trouvé de cas. L’incidence de l’AKI était plus importante dans les courses en plusieurs étapes et dans celles de durée moyenne.
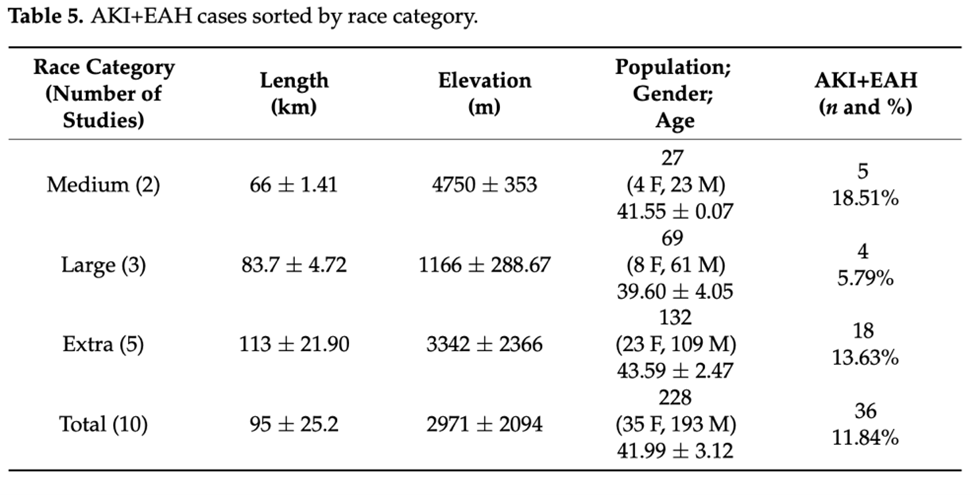
Enfin, sur 228 ultra-traileurs, 27 participants ont présenté une atteinte simultanée EAH + AKI (+9 cas étudiés qui comprenaient seulement l’EAH). La plus grande majorité des cas ont été retrouvés dans les courses d’extra longue durée.
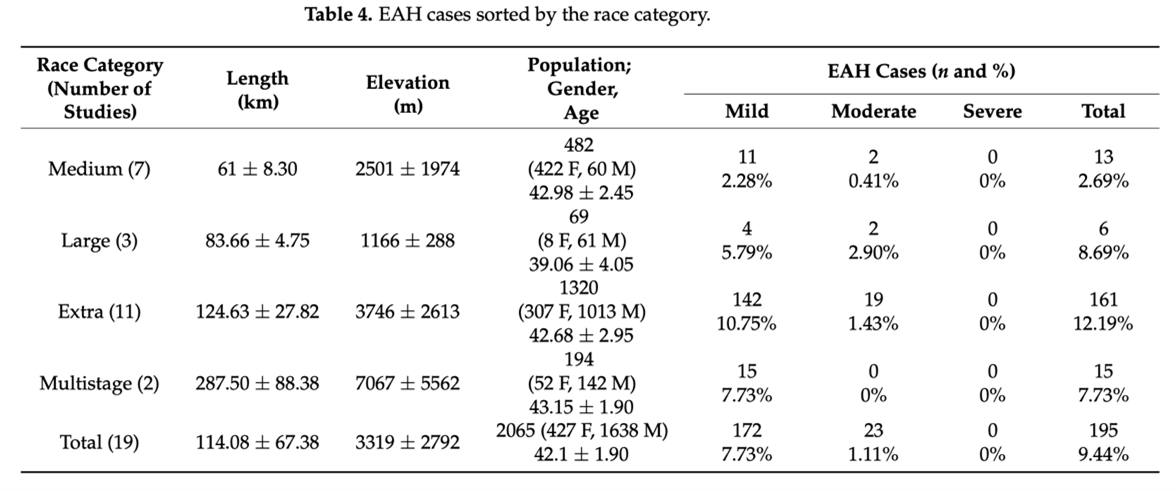
Concernant l’EAH, un total de 195 cas a été trouvé (incidence de 9,44%) dont 172 ont été classés comme hyponatrémie faible et 23 comme modérée. Il n’y a pas eu de coureur présentant une forme grave et il n’y a pas eu de cas d’hospitalisation. 7 des études analysées n’ont rapporté aucune EAH chez les participants. Les cas d’EAH étaient plus importants pour les courses d’extra longue durée. Malgré cela, des courses avec aucun cas d’hyponatrémie ont été rapportées dans toutes les catégories de distance.
Enfin, sur 228 ultra-traileurs, 27 participants ont présenté une atteinte simultanée EAH + AKI (+9 cas étudiés qui comprenaient seulement l’EAH). La plus grande majorité des cas ont été retrouvés dans les courses d’extra longue durée.
Discussion
La discussion se divisera en trois parties, la première traitant de l’AKI, la seconde de l’EAH et la dernière du développement simultané de l’AKI et l’EAH dans les ultra-trails.
AKI
Son incidence est très hétérogène, variant de 7,24% dans les longues courses à 56,66% dans les courses de moyenne distance où son incidence est maximale, ce qui pourrait s’expliquer par la vitesse de course. En effet, lors des courses de moyenne distance les vitesses des coureurs sont plus importantes ; lors d’exercices modérés le débit rénal peut chuter jusqu’à 25%, en revanche il peut chuter jusqu’à 50% lors d’exercices intenses, expliquant l’incidence élevée de l’AKI dans les ultra-trails de moyenne distance. Malgré cela, un seul participant a atteint un stade grave d’AKI, ce qui renforce les résultats de précédentes études qui suggèrent que les altérations subies par les coureurs sont transitoires et se résolvent en quelques jours sans obligation d’une intervention médicale.
L’insuffisance rénale aigüe peut parfois être difficile à diagnostiquer car ses débuts sont asymptomatiques. Les analyses de SCR (créatinine sérum) et eGFR (filtration glomérulaire) sont utilisées pour le diagnostic ; dans les études de cette revue, l’analyse la plus utilisée était la SCR alors que l’eGFR est considérée comme le gold-standard. Néanmoins certaines études ayant fait l’analyse des deux biomarqueurs ont montré des résultats différents ; certains sujets répondaient aux critères d’AKI selon le SCR mais pas selon le eGFR et inversement. Bien que les ultra-traileurs connaissent une augmentation du SCR pendant la course, son impact réel sur les lésions rénales n’est pas encore clair et cette augmentation ne pourrait être qu’une réponse physiologique de l’organisme face au stress.
Pour les courses à étapes multiples, les résultats obtenus doivent être interprétés avec prudence car les deux études qui en rapportent ont analysé des trails se déroulant dans le désert, dans lequel les conditions extrêmes de sécheresse et de température accentuent le phénomène de déshydratation.
Ces résultats, rapportés à ceux de nombreuses précédentes études analysant notamment les conditions météorologiques des trails, suggèrent que la distance et le dénivelé ne sont pas les seuls facteurs pouvant impacter l’AKI chez les coureurs. Il faudrait aussi prendre en compte la vitesse, le repos entre les courses dans les courses à plusieurs étapes, ainsi que les conditions de température et d’humidité (par exemple, les cas d’AKI sont moins fréquents lorsque les températures sont douces et l’humidité élevée).
EAH
L’incidence de l’EAH en fonction du type d’ultra-trail est plus homogène, allant de 2,69% à 12,19%, et elle semble liée à plusieurs facteurs : durée de l’exercice, vitesse lente, sexe féminin, faible poids corporel, hydratation excessive avant la course, protocole d’hydratation par des boissons hypotoniques, utilisation d’AINS et températures excessivement froides ou chaudes. Contrairement à l’AKI, le risque de souffrir d’EAH paraît augmenter avec des distances plus longues et donc des durées de courses plus importantes.
Malgré l’implication du poids corporel et de la consommation excessive de boisson (avec ou sans Na+) dans le risque de développement de l’EAH, il n’existe actuellement aucun consensus sur ces deux facteurs. La perte de poids pendant la course semble efficace pour prévenir l’EAH, et inversement la surhydratation entraine une augmentation de la masse corporelle et donc une augmentation du risque d’EAH. Les recommandations sont de 2% de perte de masse corporelle pendant la course mais certaines études ont montré des cas d’EAH pour cette valeur ainsi que pour des valeurs plus élevées. Cela peut s’expliquer par l’adaptation à l’entrainement des athlètes, qui auront des voies métaboliques plus efficaces produisant plus d’eau endogène lors de l’oxydation des substrats énergétiques. Il est important de noter que la plupart des directives indiquent que la déshydratation apparait au-delà de 3% de perte de poids et peut aussi être liée à une augmentation du risque d’EAH. Il faudra donc être vigilant sur la perte de poids ; elle est nécessaire pendant la course mais ne doit pas être excessive.
AKI + EAH
L’incidence de l’AKI associée à l’EAH était significativement plus élevée dans les courses de durée moyenne et extra-longue, ce qui est conforme aux résultats de précédentes études dans lesquelles l’incidence varie de 5 à 42%. Trois facteurs principaux augmentent le risque de développer une AKI : la rhabdomyolyse, la prise d’AINS et l’EAH. Si de nombreuses études ont étudié le lien entre rhabdomyolyse et AKI, le lien entre EAH et AKI a été moins étudié et il peut sembler vague. Malgré cela, les recherches indiquent que l’apparition simultanée de ces deux pathologies est assez fréquente.
En effet, l’hyperhydratation, identifiée comme une cause de l’EAH, crée aussi une augmentation de la rhabdomyolyse et augmente donc le risque d’AKI. Cela s’explique par l’augmentation du liquide intracellulaire lors d’un excès d’hydratation ; l’accumulation d’eau intracellulaire fragiliserait les membranes des myocytes, les rendant plus vulnérables à la rupture et la rhabdomyolyse, ce qui libérerait davantage de myoglobine et autres éléments dans la circulation sanguine. Actuellement, une seule étude de Cairns & al s’est intéressée à la concomitance EAH + AKI. Ils ont conclu qu’on ne pouvait pas affirmer que l’EAH entrainait une insuffisance rénale aigue, en revanche elle entraine une diminution de la filtration glomérulaire, qui peut potentiellement amener à une AKI sur le long terme.
Un autre facteur ayant été cité comme cause possible d’EAH et d’AKI est le dénivelé des courses, qui augmenterait la rhabdomyolyse ; plus les dénivelés seraient importants, plus la composante de travail musculaire excentrique serait prédominante. Le travail excentrique entraine une plus grande destruction cellulaire et une augmentation majorée des biomarqueurs inflammatoire. Pourtant, de précédentes études ayant analysé ces biomarqueurs ne montrent pas de différences après des ultra-trails sur terrain plat ou sur terrain accidenté avec dénivelé important. Cela serait lié à la vitesse de course qui est plus faible sur les terrains montagneux et qui compenserait la rupture musculaire se produisant à cause du dénivelé. Il est aussi important de noter que les coureurs présentant des hyponatrémies plus importantes étaient généralement ceux qui avaient le moins d’expérience sur les ultra-trails.
Conclusion
Les courses d’ultra-trails peuvent être à l’origine d’une hyponatrémie associée à l’exercice et d’une insuffisance rénale aiguë, mais leur incidence reste faible chez les sujets en bonne santé et sans antécédents. Même si ces syndromes se résolvent souvent seuls et sans complications, il est important de sensibiliser les organisateurs, entraineurs et professionnels médicaux du milieu de l’ultra-trail. L’hydratation, la consommation d’AINS, le rythme de course, le profil de la course, les caractéristiques physiques des coureurs ainsi que leur entrainement et expérience sont des facteurs déterminants dans le développement de ces pathologies. Certains mécanismes physiologiques communs à l’AKI et l’EAH pourrait favoriser leur développement simultané, la rhabdomyolyse et l’hyperhydratation jouant un rôle clé dans ce lien. Les directives actuelles servant de références pour les courses et les participants ne doivent pas être considérées comme des normes en raison de la grande hétérogénéité qui existe dans ce domaine.
Référence article
Lecina M, Castellar-Otín C, López-Laval I, Carrasco Páez L, Pradas F. Acute Kidney Injury and Hyponatremia in Ultra-Trail Racing: A Systematic Review. Medicina (Kaunas). 2022 Apr 21;58(5):569. doi: 10.3390/medicina58050569. PMID: 35629986; PMCID: PMC9146822.